Primer registro de experiencias en implante de sistemas de estimulación fisiológica en Argentina.
INVESTIGADORES:
Horacio Quiroga Ponce*, Juan Pablo Montes, Alejandro Cueto, Johnny Macías, Mauricio Abello, David Doiny, Andrés Martellotto, Sergio Dubner, Horacio Guillén, Alfredo del Río, Carlos Perona, Fernando Scazzuso, José Luis Serra, Jorge Figueroa, Ignacio Mondragón, Fernando Peñafort, Roberto Keegan, Leonardo Onetto, Fernando Senn, Omar Trotta, Jorge Secchi, Luis Barja, Juan Manuel Aboy, Federico Samlillán, Federico Robles, Daniel Ortega, Emilio Logarzo, Raúl Pérez Etchepare, Teresa Botta, Marcelo Abud, Ariel Szyzko, Javier Chaves, Julián Nicolini, Mariana Valentino, Marcelo Coll, Claudio Militello, Andrés Bochoeyer, Santiago Manzolillo, Miguel Parrapavich, Guillermo Mazo, Luis Arabia, Horacio Ruffa, Carlos Labadet, Darío Di Toro, José Luis Ramos, Laura Sanziani, Diego Velasco, Armando Pérez Silva, Alfonso Gómez, Andrés Caeiro, Alejandro Estrada, Evaristo Castellanos, Sergio González.
*Investigador principal. Jefe de sección arritmias y marcapasos del Hospital Aeronáutico Central. Recibe honorarios como asesor médico y educación en línea cardiac rhythm management, y como proctor en estimulación del sistema de conducción con herramientas Selectra 3D en BIOTRONIK SOUTHERN CONE.
Centros médicos:
Hospital Aeronáutico Central (CABA), Clínica Mariano Moreno (Moreno, provincia de Buenos Aires), Hospital Sirio Libanes (CABA), Instituto Argentino de Diagnóstico y Tratamiento (IADT, CABA), Clínica y Maternidad Suizo Argentina (CABA), Instituto Cardiovascular Buenos Aires (CABA), Sanatorio Parque (Rosario, Santa Fe), FLENI (CABA), Sanatorio Allende Cerro (Córdoba), Sanatorio Finocchieto (CABA), Sanatorio Allende Nueva Córdoba (Córdoba), Hospital Privado del Sur (Bahía Blanca, prov. de Buenos Aires), Sanatorio de la Mujer (Rosario, provincia de Santa Fe), Sanatorio La Entrerriana (Paraná, provincia de Entre Ríos), Instituto Médico de Alta Complejidad (Salta), Clínica Privada Salta (Salta), Clínica San Camilo (CABA), Hospital Universitario Austral (Pilar, provincia de Buenos Aires), Sanatorio Las Lomas (San Isidro, provincia de Buenos Aires), Sanatorio San Gerónimo (Santa Fe), Hospital Madariaga (Posadas, provincia de Misiones), Sanatorio Belgrano (Mar del Plata, provincia de Buenos Aires), Sanatorio Británico (Rosario, provincia de Santa Fe), Instituto Cardiovascular de Rosario (Rosario, provincia de Santa Fe), Sanatorio Adventista del Plata (Libertador San Martín, provincia de Entre Ríos), Clínica La Pequeña Familia (Junín, provincia de Buenos Aires), Hospital San Bernardo (Salta), Instituto Modelo de Cardiología (Córdoba), Instituto de Cardiología de Corrientes (Corrientes), Sanatorio Pasteur (San Fernando del Valle de Catamarca), Sanatorio Oulton (Córdoba), Hospital Militar Central (Ciudad de Buenos Aires), Clínica Enrique J. Carra (San Francisco, Córdoba), Hospital Privado Universitario de Córdoba (Córdoba), Insititudo de Cardiología (Tucumán), Hospital Higueras (Concepción, región del Bío Bío, Chile), Hospital del Carmen (Santiago, Chile).
RESUMEN: El presente trabajo describe los principios básicos de la estimulación del sistema de conducción, y los resultados del primer registro argentino de esta técnica de estimulación permanente. El registro comenzó en noviembre de 2020 y se encuentra actualmente en desarrollo. En la actualidad cuenta con 82 pacientes incluidos. Esta técnica, de gran aceptación mundial y permanente crecimiento local, requiere de una curva de aprendizaje, luego de la cual los resultados clínicos son alentadores y promisorios. Si bien su validación en las guías actuales de práctica clínica es parcial, existe mucha evidencia en la literatura, que probablemente implicará plena inclusión en las mismas como alternativa equivalente a la resincronización convencional. Esto impulsa a la comunidad médica internacional a desarrollarla con entusiasmo, con permanente evolución de los resultados.
ABSTRACT: this publication shows the results of the first Argentine registry of physiological permanent stimulation. The registry began in november 2020 and continues today. It currently has 82 cases. This technique, widely accepted worldwide, requires a learning curve, after which the clinical results are encouraging and promising. Although it is not yet validated in clinical practice guidelines, there is a lot of evidence in the literature that will probably imply for this technique to be considered as an alternative to biventricular resinchronization. Current results encourage the international medical community to develop conduction system pacing programs in their centers, with continuous results improvement.
INTRODUCCIÓN Y JUSTIFICACIÓN
La estimulación ventricular es globalmente aceptada y se ha realizado con gran éxito durante décadas en pacientes que presentan trastornos de generación o conducción del impulso. La evolución hacia la estimulación del sistema de conducción, también llamada “fisiológica”, ha despertado gran interés en la comunidad médica internacional en los últimos años. Si bien esta técnica ya había sido publicada en el año 2000 (1), el advenimiento reciente de herramientas que permiten lograr el posicionamiento y fijación del catéter en el área de interés permitió un gran desarrollo de programas de estimulación fisiológica en todo el mundo, demostrando la superioridad de la técnica por sobre la estimulación miocárdica del ventrículo derecho (2). Sin embargo y a pesar de la gran evidencia científica disponible, el implante del electrodo en el ápex del ventrículo derecho continúa siendo la norma actual en la gran mayoría de los implantes de marcapasos definitivo.
En los últimos años, la evidencia científica ha demostrado en forma contundente que la estimulación tradicional desde el ápex del ventrículo derecho en pacientes con disfunción sistólica ventricular se asocia, durante el seguimiento, a dilatación de los ventrículos, disfunción sistólica e insuficiencia cardíaca (3). Más aún, estudios recientes han demostrado que hasta un 25% de los pacientes sin cardiopatía estructural ni deterioro de la función sistólica del ventrículo izquierdo, luego de la estimulación ventricular, desarrollan miocardiopatía asociada a la estimulación (4), presentando este grupo de pacientes en forma significativa mayor internación por insuficiencia cardíaca y mortalidad durante el seguimiento, comparativamente con aquellos pacientes que no desarrollan cardiopatía asociada a la estimulación.
La estimulación del sistema de conducción consiste en el implante de un sistema de estimulación convencional (mismo generador, mismo catéter), en un sector específico del corazón en el cual se estimula el sistema de conducción normal, en forma exclusiva (captura selectiva), o en forma combinada entre el sistema de conducción y el miocardio circundante (captura no selectiva), en un sector anatómico-funcional posterior al sitio del bloqueo. La disociación longitudinal del sistema de conducción, por la coexistencia de fibras de los fascículos derecho, izquierdo anterior e izquierdo posterior en el sector troncular antes de la bifurcación, y la existencia de bloqueos anatómicos y funcionales previos a la división del haz de His, permite explicar la fisiopatología de la resolución del bloqueo o reclutamiento de los trastornos de conducción intraventriculares al impactar un catéter en el sistema de conducción. Esta técnica innovadora ha permitido resolver los trastornos de conducción, en lugar de hacer una simple estimulación miocárdica derecha, o el implante de dos catéteres (ventriculares derecho e izquierdo a través del seno coronario), para lograr la activación simultánea de ambos ventrículos, como sucede con la resincronización bi-ventricular tradicional. El objetivo de la estimulación fisiológica, mediante la captura del sistema His-purkinje, es lograr que el impulso estimulado alcance rápidamente el miocardio a través del sistema de conducción, con despolarización en paralelo (simultánea) de los ventrículos derecho e izquierdo, a diferencia de la despolarización en serie (primero el ventrículo derecho, luego el ventrículo izquierdo), a través del miocardio no especializado. El resultado de la estimulación fisiológica es un QRS que se asemeja en su morfología al QRS normal.
La técnica ha evolucionado en los últimos años, gracias al desarrollo de vainas y material específicos, y las indicaciones se han ampliado hacia su utilización para resincronización cardíaca (5) y la estimulación directa de la rama izquierda (6), técnicas englobadas bajo la denominación “estimulación fisiológica”. Es de destacar sin embargo que, si bien la generalización de estas técnicas ha sido rápida en centros con gran volumen de implantes, no todos los trastornos del sistema de conducción pueden ser tratados o reclutados desde la estimulación del haz de His o de la rama izquierda. Existen sin dudas indicaciones vigentes para la resincronización bi-ventricular a través del seno coronario, sobre todo para los pacientes con bloqueos parietales, distales, en los cuales la estimulación del sistema de conducción no es exitosa (7). La identificación del paciente adecuado para cada técnica debe ser estudiada cuidadosamente, con el electrocardiograma, historia clínica, estudios de imágenes, medicina nuclear, etc.
El éxito de la técnica depende de la captura efectiva del sistema de conducción con un voltaje adecuado, aunque es sabido que muchas veces se obtienen umbrales subóptimos que mejoran luego de las primeras semanas (sobre todo en la estimulación del haz de His). Como sucede en otras prácticas médicas intervencionistas, la curva de aprendizaje mejora estos resultados. La captura del sistema de conducción es confirmada por ancho de QRS, morfología y comparación con el QRS basal, pero por sobre todo por la observación de transición de la captura no selectiva al patrón selectivo o miocárdico. Para aquellos casos de umbrales de captura del miocardio y del sistema de conducción iguales o muy similares, se puede confirmar la transición a través de longitudes de ciclo de estimulación incremental, buscando disociación de ambas estructuras por refractariedad en lugar de lograrlo mediante el umbral de captura.
La estimulación fisiológica es considerada en tres escenarios diferentes: En pacientes con trastornos de conducción que requieren un marcapasos definitivo (bloqueos auriculoventriculares), pacientes con miocardiopatías y trastornos de conducción que requieren resincronización bi-ventricular, y aquellos pacientes que requieren estimulación ventricular luego de la ablación del nodo AV por fibrilación auricular de elevada respuesta ventricular con o sin cardiopatía asociada. En cuanto a los pacientes con disfunción sinusal y conducción preservada, si bien la estimulación del sistema de conducción no aporta beneficios (en general sólo requieren estimulación auricular), asegura la estimulación fisiológica ante un eventual disturbio de conducción intraventricular durante la evolución.
Las últimas guías de estimulación de la sociedad Europa de cardiología (8), se recomienda (Clase IIa) la estimulación del His como una alternativa ante el fracaso de la colocación del catéter del seno coronario para la terapia de resincronización bi-ventricular clásica. Para pacientes con dependencia de la estimulación ventricular, riesgo de subdetección ventricular o sobredetección auricular o del His en los que se considera la estimulación fisiológica, estas guías sugieren la utilización de un segundo catéter en ventrículo derecho para evitar la inhibición de la estimulación (Clase IIa). Ahora bien, en el caso de considerar el implante de un catéter adicional de seguridad en el ventrículo derecho, nos encontramos ante el mismo escenario que la resincronización bi-ventricular convencional, donde se implantan tres catéteres: uno auricular, uno de estimulación fisiológica y el ventricular de seguridad. Sin embargo, con el avance de la curva de aprendizaje, los resultados favorables y la confianza del operador en la técnica la decisión de implantar un catéter ventricular de estimulación fisiológica es cada vez menos frecuente. Esto permite implantar solamente dos catéteres para resincronización en lugar de tres catéteres (CRT-P), siendo una ventaja evidente el uso de un catéter menos. Para los pacientes que requieren terapia anti-taquicardia, el implante de un catéter ventricular es todavía imprescindible, aunque podemos continuar implantando sólo dos catéteres para terapia His – CRTD con la tecnología de detección auricular flotante, (sistema DX, Biotronik, Alemania) para aquellos pacientes que no requieren estimulación auricular. Finalmente, respecto de las guías actuales, el sujeto seleccionado para ablación del nodo AV por fibrilación auricular de alta respuesta ventricular, y sobre todo en aquellos con QRS estrecho, la estimulación del His podría estar recomendada (Clase IIb). Con igual nivel de recomendación, en el caso de BAV con fracción de eyección mayor de 40% y porcentaje estimado de estimulación ventricular superior a 40%, la estimulación del His debería ser una alternativa a la clásica estimulación del ápex de VD. Se necesitará mayor evidencia para que este tipo de terapia tenga mayor peso en la indicación de las guías de práctica clínica.
El entusiasmo y la curva de aprendizaje de la comunidad médica se asocia a una mejoría continua de los resultados. Si bien no aplicable a todos los pacientes, sin dudas que la estimulación del sistema de conducción debe ser al menos considerada en cada paciente al que indiquemos un marcapasos definitivo o resincronizador bi-ventricular.
MATERIAL Y MÉTODOS
El REGISTRO MULTICÉNTRICO ARGENTINO DE ESTIMULACIÓN DEL SISTEMA DE CONDUCCIÓN es un estudio observacional multicéntrico, en el que se han incluido e incluirán pacientes sometidos a implante de dispositivos de estimulación con vainas específicas, en posición del haz de His, rama izquierda, o variantes que se describirán más adelante. La indicación de estimulación fisiológica fue establecida por el médico tratante, sin que la inclusión en el registro influya en manera alguna en el tratamiento a recibir por el paciente.
El ingreso de los pacientes al registro se realizó al finalizar la cirugía, por medio de un formulario accesible desde el teléfono celular, que lleva escasos segundos y alimenta la base de datos en forma online y automática. A continuación (Fig. 1) se detallan los dispositivos implantados en el presente registro:
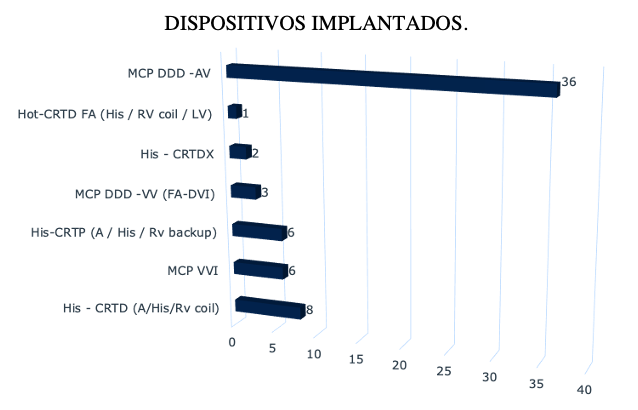
Figura 1: DISPOSITIVOS IMPLANTADOS. En orden descendente. Mcp DDD AV : marcapasos bicameral con catéteres en aurícula y en ventrículo. Hot CRTD FA: catéter en His, catéter de desfibrilación en ventrículo derecho para estimulación de seguridad y desfibrilación, catéter en ventrículo izquierdo. His-CRT DX: dispositivo con catéter ventricular de desfibrilación de coil único con detección auricular flotante sumado al catéter implantado en el sistema de conducción. Mcp DDD VV: marcapasos bicameral con catéter en His conectado al puerto auricular y catéter para estimulación de seguridad en el ventrículo derecho, en pacientes con fibrilación auricular permanente y programamdo en modo DVI. His CRTP: marcapasos tri-cameral, con catéter auricular, catéter de estimulación hisiana conectado al puerto de ventrículo izquierdo y catéter de marcapasos en ventrículo derecho para estimulación de seguridad. Mcp VVI: marcapasos unicameral implantado en el sistema de conducción. His CRTD: desfibrilador tri-cameral con catéter auricular, catéter implantado en el sistema de conducción conectado al puerto del ventrículo izquierdo y catéter de desfibrilación y estimulación de seguridad en el ventrículo derecho). La estimulación fisiológica abarca todos los dispositivos de estimulación unicameral implantado en el sistema de conducción. His CRTD: desfibrilador tri-cameral con catéter auricular, catéter implantado en el sistema de conducción conectado al puerto del ventrículo izquierdo y catéter de desfibrilación y estimulación de seguridad en el ventrículo derecho). La estimulación fisiológica abarca todos los dispositivos de estimulación
todos los dispositivos de estimulación unicameral implantado en el sistema de conducción. His CRTD: desfibrilador tri-cameral con catéter auricular, catéter implantado en el sistema de conducción conectado al puerto del ventrículo izquierdo y catéter de desfibrilación y estimulación de seguridad en el ventrículo derecho). La estimulación fisiológica abarca todos los dispositivos de estimulación
CARACTERÍSTICAS DE LOS PACIENTES
El REGISTRO MULTICÉNTRICO ARGENTINO DE ESTIMULACIÓN DEL SISTEMA DE CONDUCCIÓN incluye pacientes implantados desde el 20 de Octubre de 2020 en adelante, habiendo sido contabilizados al día de esta publicación 82 casos. La edad promedio de los pacientes fue de 61 años, con un 58% de sexo masculino. Cincuenta y nueve pacientes incluidos fueron mayores, y cinco fueron menores de 20 años (con indicación de marcapasos por bloqueo auriculoventricular completo congénito e incompetencia cronotrópica). Solo uno de los pacientes con BAVc congénito presentaba cardiopatía congénita (tetralogía de Fallot con reparación de defecto interventricular previo, cardiopatía dilatada, insuficiencia cardíaca y falla multiorgánica). En los cinco pacientes con BAV congénito se logró en forma exitosa la restauración de la conducción AV en forma fisiológica y con QRS promedio de 117 mseg, con patrón de estimulación no selectiva del haz de His. (Figuras 2 y 3). Todos los pacientes incluidos en el registro recibieron dispositivos BIOTRONIK e implante de catéteres Solia S60 a través de vainas Selectra 3D.
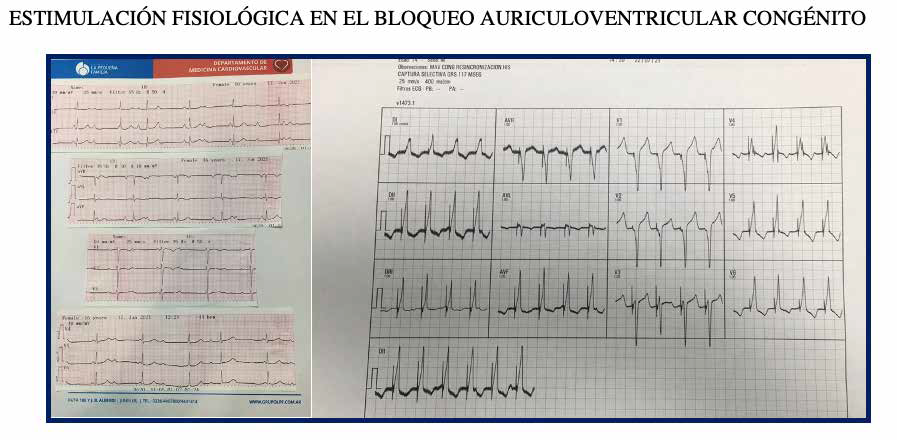
Figura 2: ESTIMULACIÓN FISIOLÓGICA EN EL BLOQUEO AURICULOVENTRICULAR CONGÉNITO Electrocardiograma de 12 derivaciones pre implante con BAV completo (izquierda), y post implante (derecha), con captura no selectiva, sin catéter ventricular de back up.
Existe consenso acerca de las dificultades de esta técnica en las etapas iniciales, y la importancia de avanzar en la curva de aprendizaje para mejorar la tasa de éxito. De esta manera, y transitando una etapa inicial de la curva de aprendizaje, la mayoría de los centros médicos priorizaron casos sencillos por sobre pacientes con trastornos de conducción más severos o distales.
Selección de la vaina adecuada y técnica de implante: La vaina Selectra 3D consta de dos diferentes curvas, la proximal que atraviesa la aurícula y la válvula tricúspide, y la distal que orienta y da soporte al catéter hacia el septum membranoso o interventricular. Consta de un lumen valvulado para la introducción del catéter y un lumen lateral para la inyección de contraste endovenoso. Es importante destacar que el catéter que se utilizó en este registro para estimulación fisiológica (Biotronik Solia S60) es exactamente el mismo que el que se utiliza habitualmente en implantes convencionales, con lumen y estilete. No es necesario ni aconsejable preformar el estilete, y este mismo junto con la vaina aportan excelente estabilidad para la fijación del catéter. En cuanto a la vaina, existen dos longitudes (32 y 39 cm), y tres curvas (40, 55 y 65 grados). Las angulaciones corresponden a la curva proximal, mientras que la curva distal (septal) es igual en todas las variantes. La vaina de longitud corta (32 cm.) puede ser utilizada en pacientes pediátricos o de contextura pequeña, aunque lo más aconsejable es siempre disponer de vainas de 39 cm. La media de vainas utilizadas en este registro fue de 1.3, observándose una clara tendencia a la menor cantidad de vainas utilizadas (una en vez de dos) a medida que se avanza en la curva de aprendizaje. La elección de la vaina depende de la anatomía del paciente y técnica de implante seleccionada. En líneas generales, se prioriza la vaina de curva más corta (40 grados) para pacientes sin dilatación auricular ni ventricular y en los que se busca la estimulación del haz de his. Esta vaina, una vez avanzada hasta el corazón, permanece casi en su totalidad en la aurícula derecha y sólo su extremo distal alcanza y atraviesa la válvula tricúspide. La vaina de 55 grados adopta una posición muy diferente a la previa, con ingreso pleno en el ventrículo derecho y posición del extremo distal algo más bajo que la de 40 grados. La vaina de curva 55 grados fue la más utilizada en este registro, siendo en nuestra experiencia la más apropiada para captura de la rama izquierda, aunque también útil en muchos casos para la captura del haz de His. La vaina de 65 grados es la menos utilizada habitualmente, reservada para pacientes con dilatación auricular y/o ventricular marcada.
En definitiva, la elección de la vaina adecuada depende inicialmente de la anatomía del paciente, de la observación de las cámaras en radioscopía y de la posición del haz de his observado a través del catéter femoral. Con estos principios la elección es adecuada en la mayoría de los casos, y más precisa cuanto con más experiencia se cuenta. La vaina adecuada será finalmente la que nos permita un posicionamiento del sistema perpendicular en 90 grados en el lugar que se desea impactar el catéter.
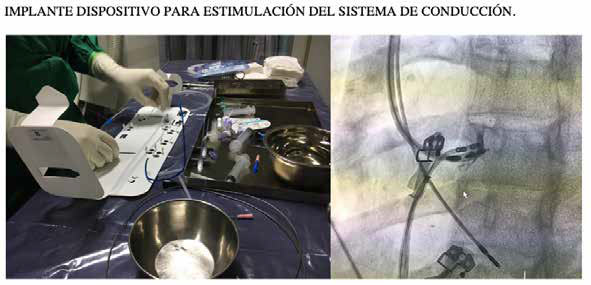
Figura 3: IMPLANTE DISPOSITIVO PARA ESTIMULACIÓN DEL SISTEMA DE CONDUCCIÓN. Vainas Selectra 3D (izquierda), inyección de contraste para determinar posición del sistema y penetración del catéter en el septum membranoso (derecha).
En cuanto a la técnica de implante, brevemente quisiéramos destacar algunos puntos importantes: el catéter se avanza inicialmente sin exponer el screw. La vaina debe ser localizada en posición perpendicular 90 grados al septum, esto confirmado por continuas inyecciones de contraste endovenoso en proyección oblicua anterior izquierda. Siendo un procedimiento de electrofisiología, no es necesario observar bajo radioscopía en forma permanente, sino guiar el mapeo por el potencial intracavitario del catéter (potencial del sistema de conducción previo al potencial ventricular con un intervalo HV aceptable). La estimulación y detección se deben analizar en forma unipolar en esta etapa, con el catéter expuesto lo mínimo indispensable para capturar el tejido, dando el mayor soporte posible al sistema catéter y estilete por parte de la vaina.
La estimulación de la rama izquierda es una técnica totalmente diferente, en la que el catéter se impacta en el septum medio, a escasos centímetros hacia delante y abajo (en vista oblicua anterior derecha) del haz de His. Una vez posicionado el catéter perpendicular al septum, y logrado el patrón de estimulación adecuado (imagen de bloqueo de rama derecha, “notch” medial en derivación V1, patrón Rs en DII y Qr en DIII), y monitoreando en forma permanente el patrón electrocardiográfico, la impedancia, la detección ventricular y el umbral de captura, se procede a impactar el catéter en forma profunda en el septum inter-ventricular, a través del giro manual en sentido horario. Los parámetros mencionados son fundamentales para que la posición final del catéter se logre dentro del septum interventricular, cercano al endocardio izquierdo, pero sin perforar el septum. El objetivo es lograr estrechamiento del QRS, aparición de patrón qR o Rs en V1, desplazamiento distal del notch en V1, y sobre todo acortamiento del tiempo desde la espiga al pico de R en V6, que siendo menor a 90 milisegundos confirma la captura de la rama izquierda (6). El principio electrofisiológico de estos hallazgos es muy simple: Al lograr la estimulación del ventrículo izquierdo en forma directa desde los fascículos del sistema de conducción, la despolarización de la cara lateral del ventrículo izquierdo (representada por la derivación V6) es temprana, en forma opuesta a lo que ocurre en el BCRI o la estimulación miocárdica derecha, donde la despolarización del ventrículo izquierdo lateral es tardío y secundario a conducción lenta a través del tejido no especializado. La técnica de estimulación de la rama izquierda permite en nuestra experiencia mejor estabilidad del catéter y mejores umbrales de captura, y por supuesto no genera inconvenientes relacionados al sobresensado o captura auricular.
Independientemente de la técnica, la fijación del catéter consta de 3 pasos: Inicialmente y una vez lograda la posición perpendicular, el potencial y patrón de estimulación deseado, se procede a la fijación activa (exposición del screw). Luego de observar nuevamente la respuesta a la estimulación, transición de patrones electrocardiográficos y umbrales de captura, se procede al segundo paso de la fijación, que consiste en el avance del cono rotador en forma firme contra el catéter, de manera de eliminar la rotación inversa del screw. Finalmente, el tercer y último paso consiste en la rotación horaria manual del catéter, con ambas manos, y guiado por radioscopía e inyección de contraste. Se procede luego a la medición de la detección ventricular, la impedancia del sistema y el patrón electrocardiográfico de captura. Al finalizar los 3 pasos y tras comprobar la correcta estimulación del sistema de conducción, la vaina debe ser retirada hasta la aurícula y la estabilidad del catéter comprobada radiológicamente, después de lo cual se procede a la extracción de la vaina. En los casos del presente registro, se utilizaron para la fijación definitiva las siguientes vainas: Selectra 3D 55-39: 40 casos, Selectra 3D 40-39: 28 casos, Selectra 3D 40-32: 4 casos, Selectra 3D 55-32: 6 casos, Selectra 3D 65-39: 4 casos.
RESULTADOS
Globalmente, el éxito de los primeros 82 implantes de este registro fue del 87%. En todos los implantes de este registro participó el investigador principal, el cual no contaba con experiencia previa. Es de destacar que, luego de sobrepasar el implante número 30, la tasa de éxito durante el implante fue superior al 95%, en concordancia con los reportes de especialistas en la materia, que coinciden en la importancia de la curva de aprendizaje. Estos resultados y consideraciones son válidos tanto para la técnica de estimulación del haz de His como para la captura de la rama izquierda.
En cuanto a los umbrales de captura, en los pacientes incluidos fue habitual observar voltajes algo más elevados que en los implantes convencionales de marcapasos, con mejoría franca luego de las primeras semanas post implante. Es por esta razón que estos dispositivos se programan inicialmente con voltaje y ancho de pulso elevados (5 V – 1.0 ms.), para luego ser optimizados durante el seguimiento. El umbral de captura del sistema de conducción en la fase previa a la penetración del electrodo debe ser tomada con cautela: si bien fue en nuestra experiencia predictor de un buen umbral luego de la fijación, en algunos casos no lo fue tanto, ya que a pesar de no presentar un umbral óptimo inicial, efectivamente el umbral fue adecuado luego de la penetración. En este sentido, la decisión de penetrar el catéter no es tomada solamente en base al umbral de captura previo a la fijación, sino además a la posición anatómica, septograma, potencial endocavitario y sensado ventricular.
En cuanto al sensado ventricular, en la técnica de implante del haz de his suele ser bajo (entre 2.5 y 4 mV.). Independientemente del valor, es esencial observar (además del potencial del haz de His) un potencial auricular mínimo o inexistente, que nos permita programar una sensibilidad ventricular (fija, no dinámica) que sense adecuadamente el ventrículo y asegure no caer en el sobresensado auricular. En caso de no ser esto posible por la magnitud del potencial auricular, el implante de un segundo catéter ventricular permitirá cegar al catéter de his y obtener back-up de sensado. Descartar la captura auricular (observando conducción decremental o disociación VA con el catéter femoral en la aurícula derecha durante las maniobras de estimulación) es siempre mandatorio durante el implante en el haz de his en general y en este escenario en particular. La técnica de estimulación de la rama izquierda presenta las enormes ventajas de evitar el riesgo de sobresensado o captura auricular.
En cuanto a la impedancia, se observan valores similares a los implantes convencionales en la técnica del haz de His. En la técnica de estimulación de la rama izquierda, monitorizar en forma continua la impedancia durante la penetración es esencial, de manera de detectar una caída brusca del valor que pudiera significar perforación septal e ingreso del catéter a la cavidad izquierda.
A continuación se detalla (Figura 4), la indicación médica del implante, así como el electrocardiograma basal de los pacientes incluidos en el registro:
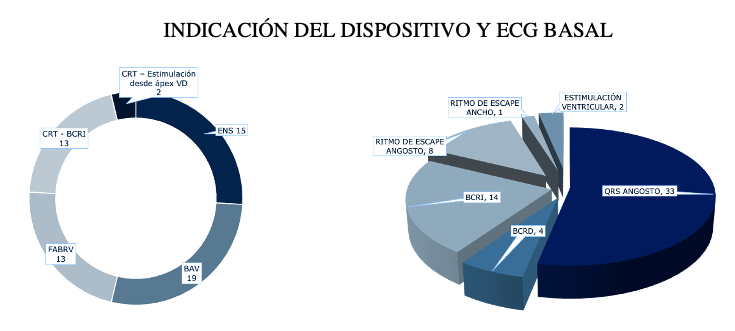
Figura 4: INDICACIÓN DEL DISPOSITIVO Y ECG BASAL A la izquierda, indicación del dispositivo, discriminando los pacientes considerados para resincronización bi-ventricular (CRT-BCRI). Estimulación disincrónica del VD y disincronía por bloqueo auriculoventricular de primer grado. ENS, enfermedad del nodo sinusal, bloqueo auriculoventricular y fibrilación auricular de baja respuesta ventricular. A la derecha, electrocardiograma basal de los pacientes.
Parámetros ecocardiográficos: La estimulación fisiológica, con la captura del sistema de conducción o a través de la resincronización biventricular tradicional, está globalmente aceptada en pacientes con disfunción ventricular. Sin embargo, los resultados electrocardiográficos y clínicos son muy alentadores aún en los pacientes con función ventricular preservada. La ausencia de cardiopatía estructural es un elemento importante por facilitar el posicionamiento y manipulación del material específico. Las guías de estimulación aún no contemplan la indicación de estimulación fisiológica en pacientes sin disfunción ventricular, aunque existe evidencia acerca del desarrollo de miocardiopatía asociada a la estimulación en pacientes con función ventricular sistólica preservada, los cuales presentan una evolución significativamente peor que los pacientes que no desarrollan cardiopatía en progresión de insuficiencia cardíaca, internaciones y mortalidad total (4).
En la población estudiada se incorporaron pacientes con función ventricular sistólica conservada y deteriorada, aunque la mayoría (56%) presentaron función ventricular normal y solo el 23% disfunción severa (fig. 5).
La anatomía cardíaca también fue variada aunque, concordante con la función ventricular, la mitad de la población tenía dimensiones normales del VI (fig. 6).
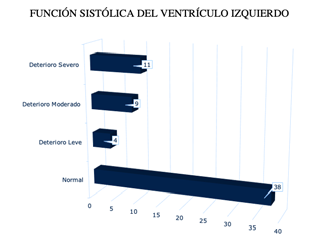
Figura 5: FUNCIÓN SISTÓLICA DEL VENTRÍCULO IZQUIERDO. Considerada en base a la fracción de eyección (mayor a 55%, normal, entre 45 y 55% deterioro leve, entre 45 y 30% deterioro moderado y menos de 30% deterioro severo).
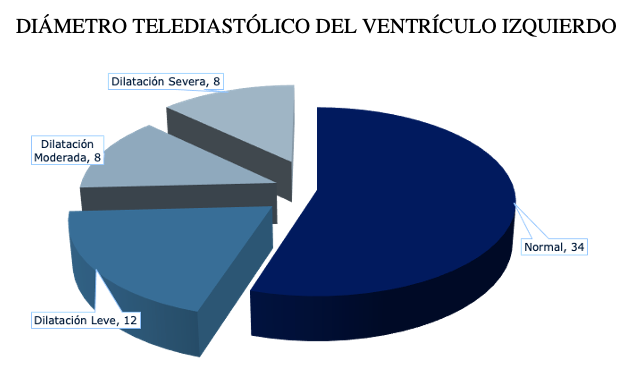
Figura 6: DIÁMETRO TELEDIASTÓLICO DEL VENTRÍCULO IZQUIERDO. Entre 42 y 59 mm, normal, entre 60 y 63 mm deterioro leve, entre 64 y 68 mm, deterioro moderado y más de 69 mm dilatación severa.
El área de la aurícula izquierda debe ser siempre evaluada y considerada sobre todo para la elección de la vaina adecuada, priorizando en principio vainas de curva más amplia en pacientes con dilatación auricular, aunque en la experiencia cotidiana se puede constatar que este concepto no es riguroso. En realidad la práctica diaria muestra que la mejor vaina es aquella que permite un contacto perpendicular al septum interventricular en el lugar deseado, dependiendo esto de conceptos más amplios de la anatomía del paciente y no puramente del diámetro auricuar. Si consideramos los diámetros auriculares de esta población veremos asimismo que 50 pacientes (60 %) tenían un diámetro auricular normal o levemente dilatado (Fig. 7)
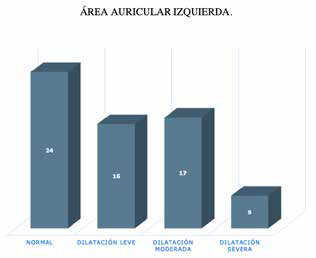
Figura 7: ÁREA AURICULAR IZQUIERDA. Valores considerados en diámetro anteroposterior: entre 30 y 40 mm, normal, entre 41 y 46 mm deterioro leve, entre 47 y 52 mm, deterioro moderado y más de 52 mm, dilatación severa.
DISCUSIÓN
El éxito de la estimulación fisiológica consiste en capturar el sistema de conducción nativo del paciente con un voltaje y ancho de pulso aceptables. La captura del sistema de conducción puede ser selectiva o no selectiva. El patrón no selectivo hace referencia a la captura del sistema de conducción y del miocardio adyacente por el mismo impulso eléctrico. La captura miocárdica es inmediata, ocurre sin retraso inmediatamente después de la espiga, y es responsable durante la captura no selectiva de la onda delta, similar a la observada en los síndromes de preexcitación ventricular. La porción subsiguiente del QRS, angosta, representa el miocardio despolarizado por el sistema de conducción, capturado en forma simultánea al miocardio pero de revelación electrocardiográfica más tardía, ya que debe transitar primero por la porción ramificante del his y el sistema His-Purkinje proximal (este retraso es equivalente al intervalo HV o, con mayor precisión, al intervalo entre el potencial del sistema de conducción sensado por el catéter y el QRS de superficie). La captura miocárdica del patrón no selectivo no ha demostrado representar una disincronía significativa, es habitualmente responsable de la despolarización sólo del miocardio circundante al catéter, y aporta estimulación de back up ante un eventual aumento patológico del umbral de captura del sistema de conducción o desarrollo de enfermedad distal al sitio de implante.
En el caso de la estimulación selectiva del fascículo de His, observamos la presencia de un QRS estimulado angosto, idéntico al basal (conducido), y un intervalo estímulo-V igual que el intervalo HV basal. Si el paciente tuviera un trastorno de conducción intraventricular (bloqueo de rama izquierda o derecha), éste deberá haber sido reclutado con el consecuente QRS angosto. Siempre se debería observar los intervalos de conducción a longitudes de ciclo incrementales, o preferentemente con extraesímulos, con el fin de estudiar la refractariedad anterógrada del tejido especializado. Si bien este patrón consta de la ventaja de estimular exclusivamente el sistema de conducción, debería ser aceptado solamente luego de evaluar cuidadosamente la integridad del mismo posterior al sitio de impacto (intervalo HV dentro de valores normales y QRS angosto o bloqueo intraventricular completamente reclutado). Si el paciente presentara un trastorno de conducción intraventricular sin reclutamiento completo, o bloqueo anterógrado por refractariedad a longitudes de ciclo no aceptables, deberíamos plantearnos reposicionar el catéter buscando un patrón de captura no selectivo, o bien implantar un catéter adicional para obtener captura miocárdica de back-up.
La experiencia de este registro nos deja la importancia de contar con un catéter por vía venosa femoral, posicionado en la región del His como una guía radiológica que permite rápidamente localizar el sitio donde implantar el catéter. Este catéter permite identificar algunos elementos de interés (potencial auricular importante, intervalo HV prolongado). Además y en la técnica de estimulación del haz de His, la recolocación del catéter femoral en posición auricular luego de la fijación permite descartar la captura auricular, comprobando conducción retrógrada decremental o disociación VA.
Para los casos de captura no selectiva de la rama izquierda en el cual el QRS no sea óptimo, debemos considerar si el catéter está adecuadamente penetrado en el septum. De todas maneras, en nuestra opinión el ancho del QRS, si bien importante en la técnica de estimulación septal profunda, es secundario al patrón de estimulación (qR en V1 y demás criterios de captura de la rama izquierda), así como el intervalo entre la espiga al pico de R en V6 (menor a 90 mseg.).
Es de destacar que la presente publicación aporta la información del implante, y durante el seguimiento contaremos con los datos que nos permitan validar la evolución clínica y electrocardiográfica de nuestros pacientes. La gran mayoría de los pacientes presentó umbrales estables o mejores de captura del sistema de conducción en los controles inmediatos y al mes del implante. Un solo paciente de este registro presentó desplazamiento del catéter, por rotación del dispositivo con tracción proximal, perdiendo la posición perpendicular respecto del septum y la captura del sistema de conducción. En este caso puntual, se intentó recolocar el catéter en la posición original sólo con el estilete, no siendo exitosos en la captura del sistema de conducción.
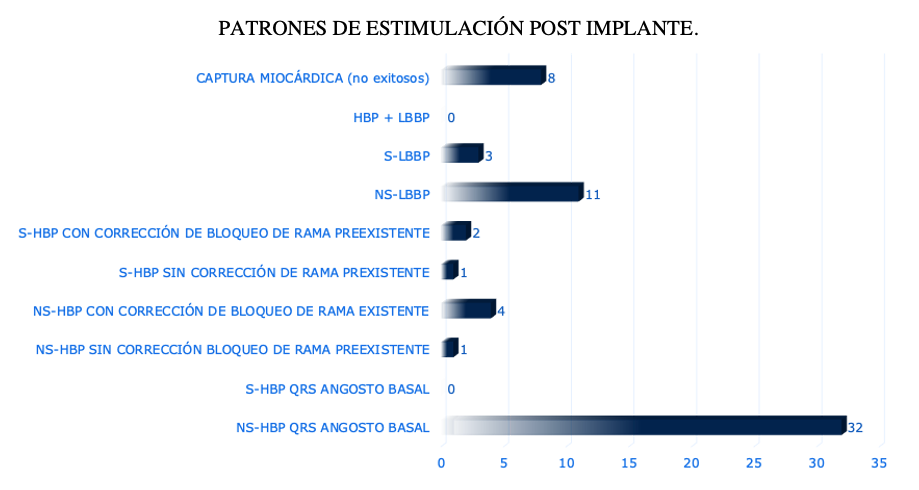
Figura 8: PATRONES DE ESTIMULACIÓN POST IMPLANTE. En orden descendente: Captura miocárdica (denominado no exitoso por no lograr el objetivo de la técnica, la captura del sistema de conducción), HBP + LBBP (estimulación del haz de his sumado a la estimulación de la rama izquierda con dos catéter diferentes, sin casos hasta ahora en la evolución del registro), S-LBBP (estimulación selectiva de la rama izquierda, sin captura miocárdica asociada), NS-LBBP (estimulación no selectiva de la rama izquierda, asociada a la captura miocárdica adicional), S-HBP con corrección de rama preexistente (estimulación pura del sistema de conducción, sin captura miocárdica, asociada a la captura de bloqueo de rama o fascicular preexistente), S-HBP sin corrección de rama preexistente (estimulación pura del sistema de conducción, sin captura miocárdica, sin captura de bloqueo de rama o fascicular preexistente. Este patrón es considerado no exitoso y pertenece a un caso con bloqueo de rama izquierda distal y estimulación miocárdica por catéter de back up), NS-HBP con corrección de bloqueo de rama preexistente (captura del haz de his y del miocardio con corrección de bloqueo de rama o fascicular preexistente), NS-HBP sin corrección de bloqueo de rama preexistente (captura del haz de his y del miocardio sin corrección de bloqueo de rama o fascicular preexistente, este caso considerado no exitoso también en escenario similar al descripto previamente), S-HBP QRS basal (estimulación selectiva del haz de his), NS-HBP QRS angosto basal (captura del his y del miocardio).
CONCLUSIONES
La estimulación del sistema de conducción es una técnica que ha logrado enorme difusión y gran aceptación en la comunidad médica. Es muy importante comprender que el éxito depende en forma crucial de la experiencia y curva de aprendizaje.. La captura no selectiva del His o de la rama izquierda permite contar con estimulación miocárdica de back-up y evitar el implante de un segundo (o tercer) catéter en el miocardio ventricular. En esta experiencia inicial de 82 casos en un año y medio de trabajo, no tuvimos complicaciones significativas y la tasa de éxito fue buena globalmente, y muy buena una vez transitados los casos iniciales. Es siempre recomendable iniciar la curva con casos más sencillos, preferentemente con conducción preservada, a fin de acostumbrarse a la técnica y herramientas, antes de pasar a los casos más complejos o con trastornos de conducción avanzados.
REFERENCIAS
- Permanent, Direct His-Bundle Pacing. A Novel Approach to Cardiac Pacing in Patients With Normal His-Purkinje Activation. 2000;101:869–877
- Sharma PS, Dandamudi G, Naperkowski A, et al. Permanent His-bundle pacing is feasible, safe, and superior to right ventricular pacing in routine clinical practice. Heart Rhythm. 2015;12(2):305–312. doi:10.1016/j.hrthm.2014.10.021
- Biventricular Pacing for Atrioventricular Block and Systolic Dysfunction. Anne B. Curtis, M.D., Seth J. Worley, M.D., Philip B. Adamson, M.D., Eugene S. Chung, M.D., Imran Niazi, M.D., Lou Sherfesee, Ph.D., Timothy Shinn, M.D., and Martin St. John Sutton, M.D, for the Biventricular versus Right Ventricular Pacing in Heart Failure Patients with Atrioventricular Block (BLOCK HF) Trial Investigators.
- Incidence and Clinical Outcomes of Pacing Induced Cardiomyopathy in Patients With Normal Left Ventricular Systolic Function and Atrioventricular Block. Omer Dor, MDa, Moti Haim, MDa,b, Orit Barrett, MDa,b,c, Victor Novack, MDa,c, and Yuval Konstantino, MDa,b,*. Am J Cardiol 2020;128:174−180
- Conduction System Pacing for Cardiac Resynchronisation. Parikshit S Sharma and Pugazhendhi Vijayaraman. Rush University Medical Center, Chicago, IL, US; 2. Geisinger Heart Institute, Wilkes-Barre, PA, US. Arrhythmia & Electrophysiology Review 2021;10(1):51–58
- Huang W. et al. A Novel Pacing Strategy With Low and Stable Output: Pacing the Left Bundle Branch Immediately Beyond the Conduction Block. Can J Cardiol 2017; 33:1736 e1-e3.
- Intracardiac Delineation of Septal Conduction in Left Bundle-Branch Block Patterns. Mechanistic Evidence of Left Intrahisian Block Circumvented by His Bundle Pacing. Gaurav A. Upadhyay, Tharian Cherian, Dalise Y. Shatz, Andrew D. Beaser, Zaid Aziz, Cevher Ozcan, Michael T. Broman, Hemal M. Nayak, Roderick Tung.
- European Heart Journal 2021; 42 (35): 3427–3520
