Ricardo Speranza1, Pablo Spaletra2, Felipe Olivieri3, Gustavo Costa4, Alberto Alfie5, Marcelo Robi5, Daniel Deluso5, Camila Olivera5, Diego Diaz5, Amílcar Ramos Barrios5, Edgardo Schmukler6, Dr. Claudio de Zuloaga7
1,5. Jefe de Servicio de Cardiología Hospital Nacional Prof. Alejandro Posadas.
2. Staff Servicio de Hemodinamia. Instituto Cardiovascular de Buenos Aires.
3. Staff de Sección de Ecocardiografía. Hospital Nacional Prof. Alejandro Posadas.
4. Jefe de Sección de Electrofisiología. Hospital Nacional Prof. Alejandro Posadas.
5. Staff de Sección de Electrofisiología. Hospital Nacional Prof. Alejandro Posadas.
6. Servicio de Cirugía Cardiovascular. Hospital Nacional Prof. Alejandro Posadas.
7. Consultor de Sección de Electrofisiología. Hospital Nacional Prof. Alejandro Posadas. Jefe de Trabajos Prácticos de Carrera de Electrofisiología
– UNLP.
Resumen. El cierre percutáneo de orejuela izquierda es una alternativa terapéutica para pacientes con fibrilación auricular y contraindicación a anticoagulación vía oral. El ecocardiograma transesofágico tiene un papel fundamental en todos los procedimientos de oclusión/exclusión percutánea de orejuela izquierda, e incluye la evaluación de la anatomía, selección del tamaño del dispositivo, su utilización como guía durante el procedimiento y el seguimiento posterior. Presentamos un caso clínico en que utilizamos el ecocardiograma transesofágico 3D como guía para el implante del dispositivo. El procedimiento fue exitoso y no se observaron
complicaciones.
Summary. Percutaneous closure of the left atrial appendage is a therapeutic choice for patients with atrial fibrillation and a contraindication for oral anticoagulation. Transesophageal echocardiography plays a fundamental role in all percutaneous left atrial appendage occlusion/exclusion procedures, allowing the anatomical evaluation, device size, also as a guide during the procedure, and subsequent follow-up. We present a clinical case in which the 3D transesophageal echocardiogram was used in our center as a guide for device implantation. The procedure was successful and no complications were seen.
Introducción
La fibrilación auricular (FA) es la arritmia más frecuente en la práctica clínica, afectando a más de 33 millones de personas en todo el mundo, y se espera que su prevalencia
se duplique en los próximos 40 años1. La FA y su capacidad embolígena se asocia a importantes eventos cardiovasculares adversos como el accidente cerebrovascular (ACV) grave determinando que sea una de las arritmias cardiacas con mayor impacto sociosanitario, por la morbi- mortalidad asociada que sobrelleva. Existe evidencia consistente sobre la reducción del riesgo de complicaciones tromboembólicas con la utilización de anticoagulantes orales, aunque también son conocidos sus potenciales riesgos, como las hemorragias2-4.
La orejuela izquierda (OI) es el sitio de origen más común de formación de trombos en la fibrilación auricular no valvular, es así que el 90% de los trombos asientan en esta estructura. Esto ha llevado a desarrollar sistemas mecánicos para la oclusión de la misma y de esta manera prevenir el accidente cerebrovascular (ACV). En nuestro país el cierre percutáneo de la OI está experimentando un crecimiento gradual, siendo una alternativa terapéutica para pacientes con fibrilación auricular no valvular y contraindicación al tratamiento anticoagulante.
Correspondencia: Ricardo Speranza
Email: ricardo.speranza@yahoo.com
Recibido: 12/05/2022 Aceptado: 22/06/2022
Caso Clínico
Paciente de 73 años, sexo femenino, antecedentes de hipertensión arterial, diabetes tipo II, fibrilación auricular paroxística anticoagulada con acenocumarol, que ingresó a
nuestro centro por presentar afasia de Broca y hemianopsia derecha, observándose controles de anticoagulación en rango terapéutico. La TAC de encéfalo mostró área hipodensa cortico subcortical frontal derecha que genera borramiento de los espacios y surcos subaracnoideos adyacentes, compatible con evento vascular isquémico agudo/subagudo en territorio de arteria cerebral anterior. La RMN confirma el ACV isquémico, aunque evidencia además zonas de transformación hemorrágicas.
Paciente con CHA2DS2VASC 6 Y HAS-BLED 3. Se realizo evaluación conjunta con equipo multidisciplinario decidiéndose el cierre percutáneo de orejuela izquierda con
dispositivo oclusor.
Se realiza evaluación de anatomía de la orejuela izquierda mediante ecocardiograma transesofágico en los siguientes ángulos, 0, 45, 90 y 130° para determinar morfología, mediciones del ostium, y descartar la presencia de trombos (Figura 1).
Descripción de Procedimiento. Por acceso venoso femoral derecho se introduce set de punción transeptal, accediéndose a aurícula izquierda bajo guía ecográfica, ecocardiograma transesofágico (ETE) 3 D (X plane), para lograr una punción inferior y más posterior del septum interauricular que es el sitio óptimo para un abordaje más directo a la zona de interés (Figura 2). Se completa dosis plena de anticoagulación con heparina sódica ev.
Posteriormente se coloca guía en la vena pulmonar superior izquierda, para realizar intercambio de vaina. Se introduce sistema de posicionamiento de dispositivo 14 F, se coloca pigtail accediendo a orejuela de AI. Se realiza angiograma con contraste (proyecciones en RAO 30 —craneal 20 y RAO 30— caudal 20) y mediciones de la misma con ETE 2D y 3D. (Figura 3).
Se determina la medida del dispositivo a utilizar y se avanza el mismo a través de la vaina de posición (Figura 4). Se comprueba correcto posicionamiento del dispositivo (Figura 5) sin leak en el doppler cardiaco y luego de tomar las determinaciones necesarias de posición y sujeción (PASS), se decide la liberación del dispositivo (WATCHAMAN FLX 27 MM –BOSTON SCIENTIFIC) evidenciando su adecuado posicionamiento. Se realiza nuevo control ecográfico para determinar posicionamiento de dispositivo con imagen 3D y Doppler que determina ausencia de fuga (leak) peridispositivo (Figuras 6 y 7). Finalmente se realiza imagen final radioscópica del dispositivo ya implantado donde se observa un adecuado despliegue del mismo (Figura 8).
La paciente evoluciona favorablemente sin complicaciones y es externada a las 24 hs indicándose doble antiagregación.
Discusión
La necesidad de iniciar una terapéutica antitrombótica en pacientes con FA crónica y riesgo elevado para ACV puede verse comprometida en ciertas situaciones que dificultan la utilización de anticoagulantes convencionales (antagonistas de la vitamina K) o nuevos anticoagulantes (NOAC), como antecedentes de hemorragia intracraneana o ACV hemorrágico, presencia de coagulopatías, eventos isquémicos recurrentes a pesar de niveles terapéuticos de warfarina o buena adherencia a nuevos anticoagulantes (considerado como falla terapéutica), entre otras. El cierre percutáneo de orejuela izquierda (CPOI) con dispositivo WATCHMAN demostró ser no inferior al tratamiento con Warfarina en dos estudios randomizados para el objetivo primario (combinado de accidente cerebrovascular, embolia sistémica y muerte cardiovascular o no explicada), con una tasa de eventos periprocedimiento no menor, con una incidencia de derrame pericárdico grave del 4,4%.5-7 Además, se observó menor tasa de sangrado en los pacientes que continuaron en seguimiento8. Estos datos fueron validados en un metaanálisis a nivel de pacientes de los dos ensayos randomizados y
sus registros asociados9.
El registro Ewolution reportó una alta tasa de éxito de implantación (98%), con una tasa aceptable de complicaciones relacionadas con el procedimiento del 4% a 30 días10. El PRAGUE-1711, comparó la utilización de NOACs vs. CPOI en pacientes con FA crónica no valvular con alto riesgo de presentar un ACV (CHA 2D S 2 – VA S c: 4. 7). PRAGUE- 17 es el primer ensayo multicéntrico y aleatorizado para recibir CPOI (n = 201) o NOAC (n = 201), para la prevención de ACV por cualquier causa, embolia sistémica,
muerte cardiovascular, sangrado clínicamente significativo y complicaciones relacionadas con el dispositivo/procedimiento. Se logró un éxito en el implante del dispositivo en el 90% de los casos. Los dispositivos implantados fueron Amulet, Watchman o Watchman-FLX en 61,3%, 35,9% o 2,8%, respectivamente. En el grupo NOAC, apixaban se utilizó con mayor frecuencia (95,5%). En una mediana de 19,9 meses de seguimiento, las tasas anuales para el punto final primario fueron del 10,99% con CPOI y 13,42% con NOAC (cociente de riesgo de subdistribución [sHR]: 0,84; intervalo de confianza [IC] del 95%: 0,53 a 1,31; p = 0,44; p = 0,004 para no inferioridad). Este estudio concluyó que entre los pacientes con alto riesgo de accidente cerebrovascular y mayor riesgo de sangrado, el CPOI no fue inferior a NOAC en prevención de eventos cardiovasculares, neurológicos y hemorrágicos relacionados con la FA.
Recientemente el estudio PINNACLE FLX (Protection Against Embolism for Nonvalvular AF Patients: Investigational Device Evaluation of the Watchman FLX LAA
Closure Technology), evaluó la seguridad y efectividad del dispositivo de siguiente generación WATCHMAN FLX para el cierre de OI en pacientes con FA no valvular en
quien la anticoagulación oral es indicada pero que tienen una justificación adecuada para buscar una alternativa no farmacológica. Se evaluaron prospectivamente 400 pacientes, no randomizados, observándose una baja incidencia de efectos adversos y una alta incidencia de cierre anatómico12. De acuerdo con las recomendaciones actuales de las guías europeas, la oclusión de OI podría ser considerada para prevención de ACV en pacientes con FA y contraindicación del tratamiento anticoagulante a largo plazo (CLASE II B)13.
En nuestra experiencia inicial reportada utilizamos el ETE 2D y la angiografía contrastada de la orejuela izquierda durante el procedimiento para la valoración anatómica, la
elección del dispositivo y su adecuado posicionamiento 14,15. En nuestro último caso utilizamos el ETE 3D como guía para el implante del dispositivo, siendo de gran aporte
durante la punción transeptal, la elección del dispositivo ya que permite estimar mejor el tamaño del mismo, y para una mejor visualización de la zona de anclaje. Posterior al posicionamiento del dispositivo se debe realizar Doppler para descartar fugas (leak) peridispositivo. Se acepta un valor de leak residual < 5 mm.
Varios grupos de trabajo han utilizado el ETE 3D como guía para el implante del dispositivo, para evaluar la característica anatómica, la dimensión de la zona de aterrizaje
y la profundidad de la OI. Sobre esta base, se lleva a cabo la selección del dispositivo de cierre. Durante el procedimiento, es utilizado para guiar la punción del tabique interauricular, el posicionamiento del dispositivo y evaluar los efectos de la oclusión16,17
La carga de volumen antes del cierre de la orejuela aumenta significativamente las dimensiones de la misma. Las mediciones de la orejuela izquierda con ETE 3D muestran
una correlación más estrecha con el tamaño del dispositivo oclusor que las mediciones con ETE 2D o angiográficas18.
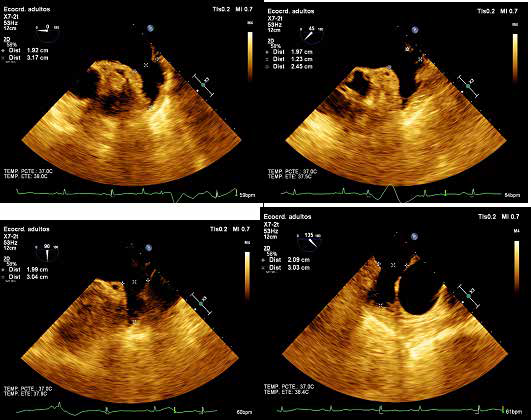
Figura 1. Mediciones por ecocardiografía transesofágica de orejuela izquierda en diferentes ángulos (0, 45, 90 y 135º) para evaluación morfológica, mediciones a nivel del ostium, y descartar trombos en el interior de la misma.
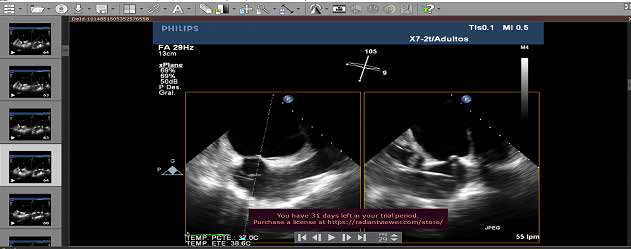
Figura 2. Punción transeptal guiada por ecocardiograma transesofágico tridimensional (X plane 45 y 135°) en región inferior y posterior de la fosa oval del septum interauricular (tenting en SIA). AI; auricula izquierda, SIA: septum interauricular.
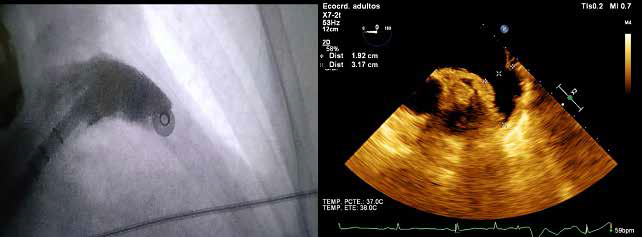
Figura 3. A la izquierda se observa angiografía contrastada de orejuela izquierda (RAO 30 —craneal 20), y a la derecha mediciones de orejuela izquierda a nivel del ostium por ETE.
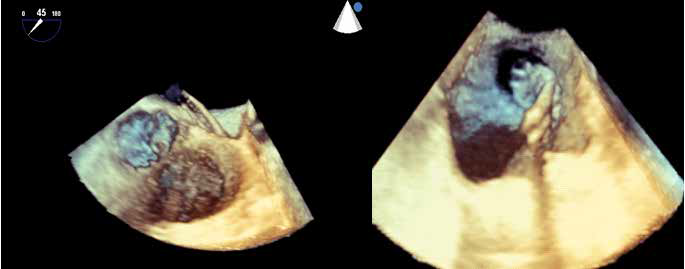
Figura 4. Ecocardiograma transesofágico 3D. Se visualiza ingreso de sistema de liberación de dispositivo (flecha) en orejuela izquierda. V Ao: Válvula aortica, VM: Válvula mitral.
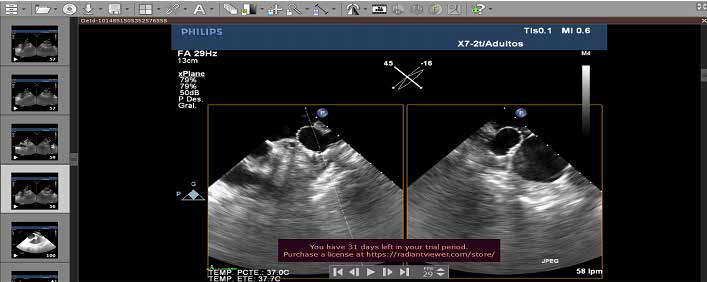
Figura 5. Posicionamiento de dispositivo Watchman FLX (previo a liberación). OI: Orejuela izquierda.
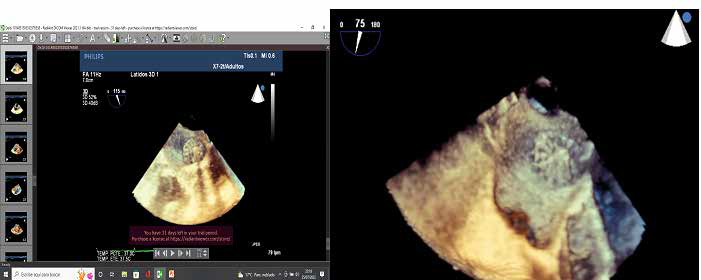
Figura 6. Ecocardiograma transesofágico 3D. Se observa dispositivo Watchman FLX implantado en orejuela izquierda.
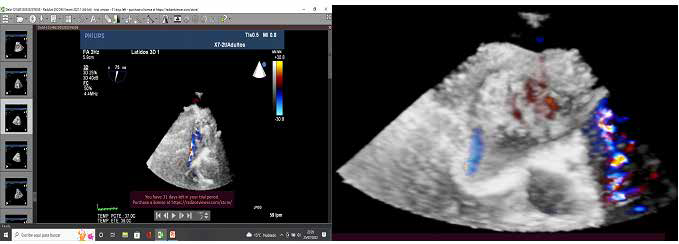
Figura 7. Ecodoppler que muestra ausencia de leak periprotésico.

Figura 8. Imagen radioscópica de dispositivo Watchman FLX implantado.
Conclusiones
Presentamos el caso clínico de una paciente que se le realizó un CPOI con dispositivo Watchman FLX, mostrando el aporte del ETE 3D como guía para el implante del mismo siendo de gran interés para precisar el sitio de punción del tabique interauricular, en la elección del dispositivo y su posicionamiento y para evaluar los efectos de la oclusión. Contar con esta herramienta garantiza un procedimiento más efectivo y seguro.
Agradecimientos
Agradecemos a los fellows en electrofisiología Diego Costa, Iván Franco, y Gustavo Gómez, a los Técnicos en Prácticas Cardiológicas Ana María Caro, Natalia Paradisi, Erika Paradisi, y Cristian Barrionuevo, y al plantel de enfermería Lic. Gabriela Cervetto, Analía Bravo, Julio Echegoyen y Javier Jara por su colaboración y dedicación incondicional.
Referencias
1. Chugh SS, Havmoeller R, Narayanan K, et al. Worldwide epidemiology of atrial fibrillation: a global burden of disease 2010 study. Circulation 2014; 129:837–47.
2. Ruff CT, Giugliano RP, Braunwald E, et al. Comparison of the efficacy and safety of new oral anticoagulants with warfarin in patients with atrial fibrillation: a meta-analysis of randomised trials. Lancet 2014; 383:955–62.
3. Christian T Ruff, Robert P Giugliano, Eugene Braunwald, et al. Comparison of the Efficacy and Safety of New Oral Anticoagulants With Warfarin in Patients With Atrial Fibrillation: A Meta-Analysis of Randomised Trials. Lancet. 2014,15; 383:955-62.
4. Freedman B, Martinez C, Katholing A, et al. Residual risk of stroke and death in anticoagulant-treated patients with atrial fibrillation. JAMA Cardiol 2016; 1:366–8
5. Fountain RB, Holmes DR, Chandrasekaran K, et al. The PROTECT AF (WATCHMAN Left Atrial Appendage System for Embolic Protection in Patients with Atrial Fibrillation) trial. Am Heart J 2006; 151: 956-961.
6. Reddy VY, Sievert H, Halperin J, et al. PROTECT AF Steering Committee and Investigators. Percutaneous left atrial appendage closure vs warfarin for atrial fibrillation: a randomized clinical trial. JAMA 2014; 312:1988-1998.
7. Holmes DR Jr, Kar S, Price MJ, Whisenant B, Sievert H, Doshi SK, Huber K, Reddy VY. Prospective randomized evaluation of the Watchman Left Atrial Appendage Closure device in patients with atrial fibrillation versus long-term warfarin therapy: the PREVAIL trial. J Am Coll Cardiol 2014; 64:1–12.
8. Reddy VY, Mobius-Winkler S, Miller MA, et al. Left atrial appendage closure with the Watchman device in patients with a contraindication for oral anticoagulation: the ASAP study (ASA Plavix Feasibility Study With Watchman Left Atrial Appendage Closure Technology). J Am Coll Cardiol 2013; 61:2551–2556.
9. Reddy V.K.,Doshi Saibal, Kar Douglas et al. 5-Year Outcomes After Left Atrial Appendage Closure: From the PREVAIL and PROTECT AF Trials. J Am Coll Cardiology 2017;24: 2976-2978.
10. Boersma LV, Schmidt B, Betts TR, et al. Implant success and safety of left atrial appendage closure with the WATCHMAN device: periprocedural outcomes from the EWOLUTION registry. Eur Heart J 2016; 37:2465-2474.
11. Pavel Osmancik, Dalibor Herman, Petr Neuzi et al. Left Atrial Appendage Closure Versus Direct Oral Anticoagulants in High-Risk Patients With Atrial Fibrillation. JACC. 2020,75:3122- 35
12. Saibal Kar , Shephal K Doshi , Ashish Sadhu ,et al. Primary Outcome Evaluation of a Next-Generation Left Atrial Appendage Closure Device: Results From the PINNACLE FLX Trial. Circulation. 2021 May 4;143(18):1754-1762.
13. G. Hindricks et al. Guía ESC 2020 sobre el diagnóstico y tratamiento de la fibrilación auricular, desarrollada en colaboración de la European Association for Cardio-Thoracic Surgery (EACTS). Rev Esp Cardiol. 2021;74(5): 437.e1–437.e1
14. Ricardo Speranza, Alberto Alfie, Claudio de Zuloaga y col. Experiencia inicial en cierre percutáneo de orejuela izquierda. Rev Electro y Arritmias 2018; 10: 56-61.
15. Dr. Ricardo Speranza Dr. Claudio de Zuloaga. Eficacia y seguridad del cierre percutáneo de la orejuela izquierda. Revista Argentina de Cirugía Cardiovascular – Volumen XVIII – Número 2- Pág. 76-82.
16. Vainrib AF, Harb SC, Jaber W, et al. Left Atrial Appendage Occlusion/ Exclusion: Procedural Image Guidance with Transesophageal
Echocardiography.J Am Soc Echocardiogr. 2018 Apr;31(4):454-474. doi: 10.1016/j.echo.2017.09.014. Epub 2017 Nov 20
17. Qing Zhou 1, Hongning Song, Lan Zhang et al. Roles of real-time three-dimensional transesophageal echocardiography in peri-operation of transcatheter left atrial appendage closure. Medicine (Baltimore). 2017 Jan;96(4):e5637. doi: 10.1097/MD.0000000000005637
18. Baravan Al-Kassou, Apostolos Tzikas, Friederike Stock, et al. A comparison of two-dimensional and real-time 3D transoesophageal echocardiography and angiography for assessing the left atrial appendage anatomy for sizing a left atrial appendage occlusion system: impact of volume loading. EuroIntervention. 2017 Apr 20;12(17):2083-2091.
